Dedicado a José Juan García Marín
Todo ser humano, si se lo propone, puede ser escultor de su propio cerebro.
Santiago Ramón y Cajal
Esta célebre afirmación de Santiago Ramón y Cajal, pronunciada en los albores de la neurociencia, trascendió la mera metáfora sobre la educación y la voluntad para convertirse en una profecía biológica literal. Durante décadas, la investigación sobre el deterioro cognitivo se enclaustró en el sistema nervioso central (SNC), observando el cerebro como una fortaleza aislada. Hoy, la ciencia contemporánea nos demuestra que ese santuario está en comunicación constante con los sistemas periféricos, y que el ejercicio físico es el cincel fundamental con el que el cuerpo humano esculpe y protege su red neuronal.
Hace cinco días, el espíritu de la predicción de Cajal encontró un asombroso eco molecular. Investigadores de la Universidad de California, San Francisco (UCSF), publicaron en la revista Cell el mecanismo exacto que explica cómo el movimiento corporal protege el cerebro. El estudio define un eje vital entre el hígado y el cerebro: el esfuerzo físico induce la secreción hepática de la enzima fosfolipasa D1 específica de glicosilfosfatidilinositol (GPLD1). Esta proteína viaja a través del torrente sanguíneo para blindar la barrera hematoencefálica (BHE) al escindir una molécula destructiva: la fosfatasa alcalina inespecífica de tejido (TNAP).
La muralla del santuario: Fisiología y vulnerabilidad de la barrera hematoencefálica
Para comprender la magnitud de este descubrimiento, debemos asomarnos a la microanatomía de la frontera cerebral. La BHE es una interfaz vascular altamente selectiva que separa el cerebro de la circulación sistémica, formada por un mosaico celular inexpugnable: células endoteliales microvasculares cerebrales (BMEC), astrocitos y pericitos.
A diferencia de otros vasos sanguíneos, las BMEC carecen de poros o fenestraciones. Están selladas por uniones estrechas (compuestas por proteínas como claudinas y ocludinas), que restringen severamente el paso de sustancias, permitiendo solo la entrada de nutrientes esenciales y orquestando la expulsión meticulosa de neurotoxinas como el amiloide-beta.
La brecha del tiempo y la neuroinflamación
El envejecimiento, sin embargo, asedia esta fortaleza. Con el paso de los años, las uniones estrechas se degradan estructuralmente, dando lugar a una barrera hiperpermeable.
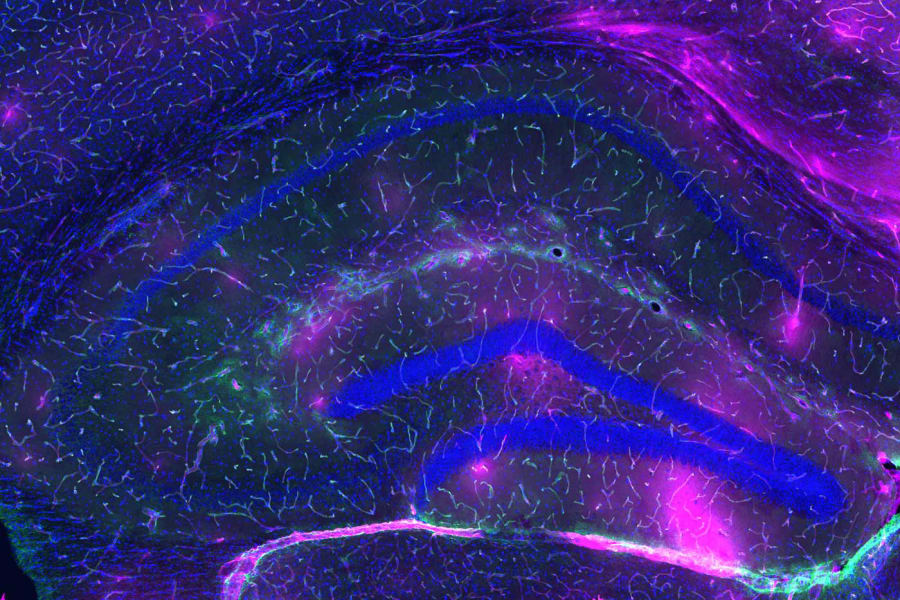
Para medir la magnitud de esta degradación en el laboratorio, los científicos no observan murallas de piedra, sino el flujo de marcadores microscópicos. Evalúan la velocidad exacta a la que fluidos y moléculas, como si fueran invasores cruzando un foso, logran traspasar el endotelio celular. Lo que en la juventud era un sello biológico hermético y casi inexpugnable, con la senescencia se convierte en un tamiz permisivo. A través de estas brechas estructurales, las células inmunitarias periféricas y las citoquinas inflamatorias logran penetrar en el cerebro.
Esta infiltración desata una tormenta de neuroinflamación crónica que hiperactiva la microglía y altera el delicado ecosistema en el que habitan las neuronas, aquellas a las que Cajal bautizó poéticamente como “las misteriosas mariposas del alma”. Este asedio inflamatorio acelera la acumulación de proteínas patológicas, precipitando la ruina cognitiva característica de enfermedades como el Alzheimer y el Parkinson.
La herrumbre molecular: Fosfatasa alcalina inespecífica de tejido (TNAP)
El principal mediador de esta degradación no es un invasor externo, sino una enzima propia que se acumula patológicamente con la edad: la TNAP, anclada a la membrana de las células endoteliales por un resto lipídico.
De escultor óseo a destructor vascular
En un organismo joven, la TNAP es una aliada vital: regula la mineralización de nuestros huesos descomponiendo moléculas que inhiben la calcificación (el pirofosfato inorgánico) para transformarlas en los bloques de fosfato que dan dureza y estructura al esqueleto.
No obstante, al envejecer, los mamíferos acumulan niveles tóxicos y fuera de lugar de esta misma enzima en la superficie de los microvasos cerebrales. Este exceso enzimático actúa como un óxido biológico que desmantela las proteínas que unen a las células, socavando los cimientos de la barrera hematoencefálica y disparando su permeabilidad. El equipo de UCSF demostró de forma concluyente que ratones jóvenes, genéticamente modificados para sobreexpresar TNAP en su barrera cerebral, perdían rápidamente sus capacidades cognitivas, confirmando que la acumulación de esta proteína es un artífice directo de la senescencia mental.
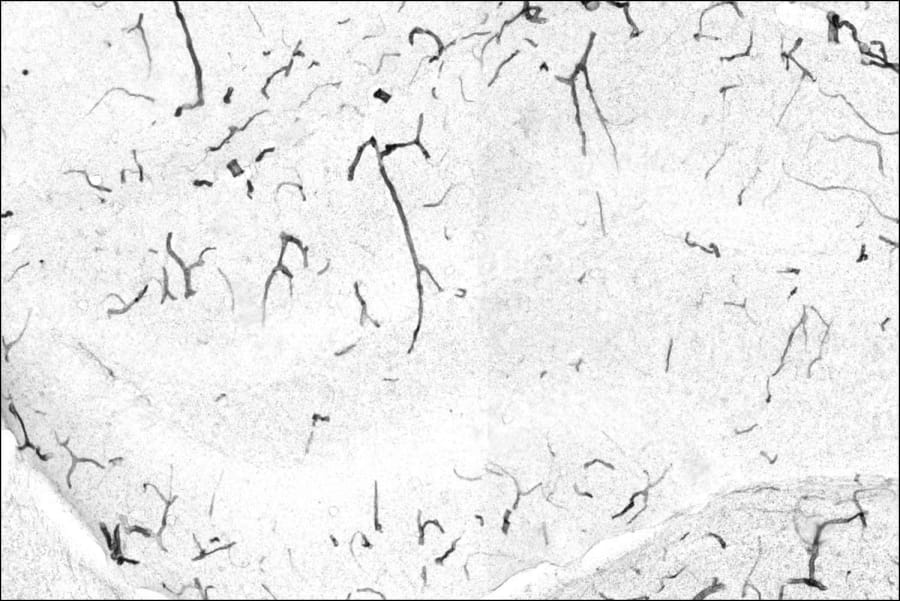
El cincel de la voluntad: El eje GPLD1 y el rejuvenecimiento
Si hay algo en nosotros verdaderamente divino, es la voluntad. Por ella afirmamos la personalidad, templamos el carácter, desafiamos la adversidad, reconstruimos el cerebro y nos superamos diariamente.
Es precisamente la voluntad humana, materializada en el esfuerzo del ejercicio físico, la que desencadena el antídoto contra el declive. La comprensión de este mecanismo nació de los estudios de parabiosis heterocrónica, que demostraron cómo la sangre joven o ejercitada encierra factores capaces de rejuvenecer un cerebro anciano.
El hallazgo de 2020 señaló a la enzima hepática GPLD1 como la mensajera principal de este milagro biológico. Sin embargo, se cernía una paradoja: la GPLD1 es demasiado grande para atravesar la BHE e ingresar al cerebro.
La restauración de las murallas
El estudio definitivo de 2026 resolvió el enigma demostrando que la GPLD1 no necesita entrar al santuario para protegerlo; libra su batalla en la periferia. Impulsado por el ejercicio, el hígado vierte GPLD1 en la sangre. Al alcanzar los vasos cerebrales, esta enzima actúa como una “tijera molecular” que recorta y libera a la perjudicial TNAP, arrancándola de las paredes vasculares.
Los resultados son asombrosos. Al administrar GPLD1 a ratones geriátricos (equivalentes a humanos de 70 años), la arquitectura de la barrera se restauró instantáneamente. La neuroinflamación se extinguió y los animales recuperaron una memoria y agilidad mental propias de su juventud.
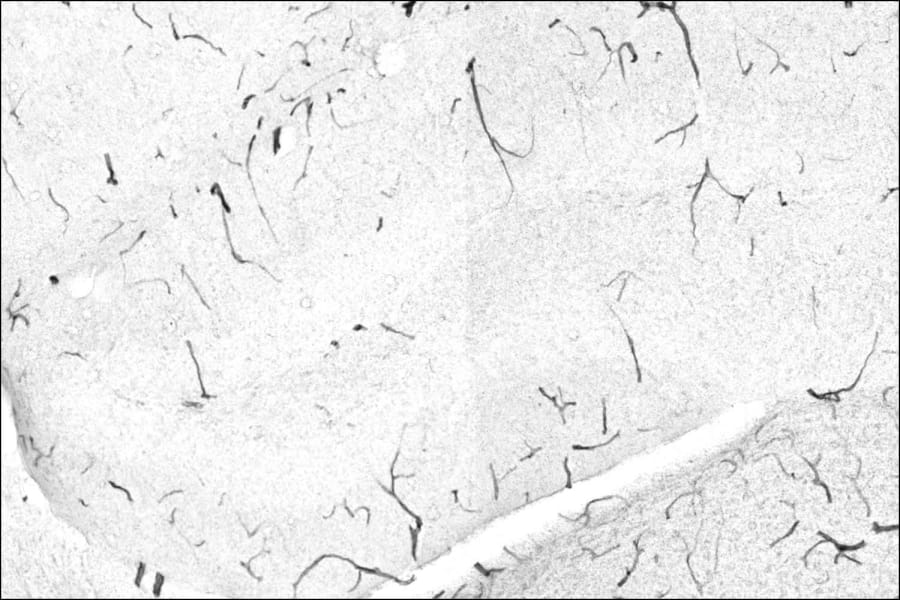
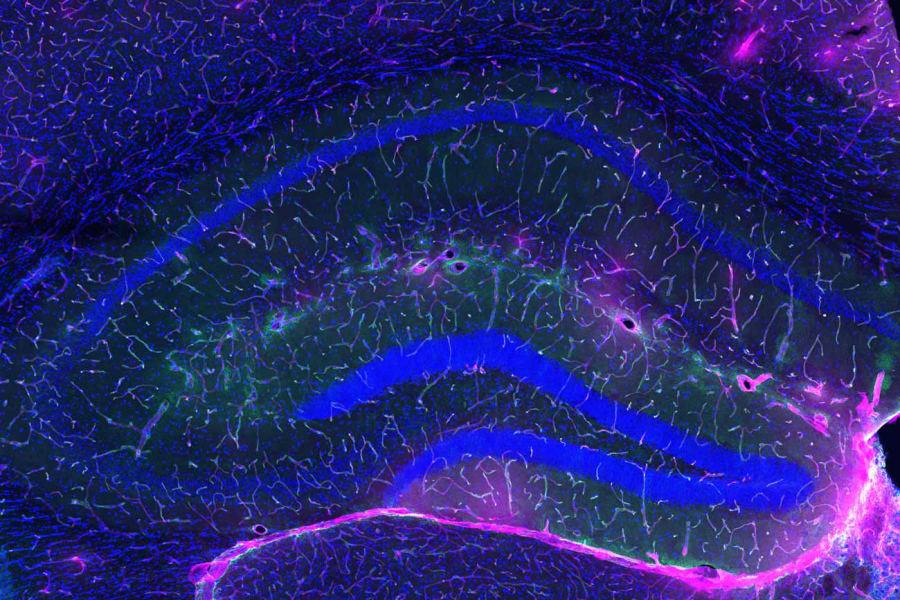
Proteína / EnzimaÓrgano de origenLocalización objetivoFunción principal / Mecanismo de acciónImplicación en el envejecimiento cognitivo****GPLD1HígadoTorrente sanguíneo (no cruza la BHE)Escinde proteínas ancladas en superficies celulares.Aumenta con ejercicio; recorta TNAP de la BHE, reduciendo neuroinflamación.TNAPCélulas endoteliales microvascularesVasos cerebrales (luminal y abluminal)Ectoenzima reguladora de mineralización e integridad endotelial.Se acumula patológicamente con la edad, destruyendo uniones estrechas.Tabla 1: Resumen de los efectores moleculares primarios en el eje vascular hígado-cerebro.
La sinfonía del cuerpo: Interacción multisistémica
La reparación mediada por la GPLD1 es solo un instrumento dentro de la orquesta de las exequinas (factores liberados durante el ejercicio). Mientras moléculas fascinantes como el factor neurotrófico derivado del cerebro (BDNF) cultivan el nacimiento de nuevas neuronas en el interior del tejido, la GPLD1 asegura las fronteras. Al sellar la barrera hematoencefálica, la GPLD1 silencia la inflamación del resto del cuerpo, creando un remanso de paz inmunológica en el cerebro que permite a estas nuevas neuronas florecer y conectarse en toda su plenitud.
El desencadenante de esta cadena es un asombroso diálogo químico: el esfuerzo agotador del músculo produce compuestos energéticos (como los cuerpos cetónicos) que viajan hasta el hígado, ordenándole fabricar la GPLD1. Esta danza celular entrelaza evolutivamente el sudor del músculo, el vigor del hígado y la protección de los recuerdos.
Alterando el “cruel decreto”: Inhibidores farmacológicos de la TNAP
“Los circuitos nerviosos son algo fijo, cerrado e inmutable. Todo puede morir, pero nada puede regenerarse. Es tarea de la ciencia del futuro modificar este cruel decreto.”
Para millones de ancianos cuya fragilidad física les impide el esfuerzo vigoroso, la ciencia del futuro —ahora nuestro presente— ha forjado un mimético de la voluntad. Si la misión de la GPLD1 es eliminar la TNAP, el desarrollo de fármacos que inhiban directamente a esta enzima destructora podría encapsular en una pastilla los beneficios neurológicos del ejercicio.
El candidato SBI-425 y el reto fisiológico
El inhibidor selectivo SBI-425 representa este paradigma. Por un elegante diseño de seguridad, esta molécula actúa únicamente en las paredes externas de los vasos sanguíneos y no cruza hacia el interior del cerebro sano, bloqueando así a la TNAP patológica sin perturbar el frágil equilibrio de las neuronas. En modelos de Alzheimer severo, el tratamiento con SBI-425 selló las fugas vasculares, redujo drásticamente las placas tóxicas de amiloide y devolvió la vitalidad a los sujetos.
El camino clínico, no obstante, exige la misma prudencia que guio la carrera del Sabio. La inhibición sistémica prolongada de la TNAP debe calibrarse con una precisión exquisita para proteger la barrera cerebral sin frenar excesivamente la mineralización de los huesos (un riesgo latente de osteomalacia), buscando el equilibrio perfecto que brinde luz a las mentes marchitas.
Inhibidor de TNAPMecanismo y selectividadPenetración de BHERiesgos sistémicos identificadosEstado de investigación****SBI-425Inhibición selectiva de molécula pequeña.No cruza la BHE sana.Riesgo de supresión de formación ósea.Éxito in vivo en modelos murinos de Alzheimer.MLS-0038949Inhibición de arilsulfonamida específica.Indeterminado.Efectos desconocidos en hueso/hígado.Evaluación preclínica inicial in vitro.L-p-BTInhibidor pan-TNAP.Indeterminado.Interrumpe vasoconstricción adrenérgica.Ensayos de reactividad mesentérica.Tabla 2: Perfil de inhibidores experimentales de la TNAP.
El paisaje clínico de 2026 y la prescripción de la longevidad
En la actualidad, la vanguardia contra la neurodegeneración avanza en múltiples frentes poli-farmacológicos (como los ensayos AR1001, Buntanetap, o las audaces plataformas de Denali Therapeutics que buscan transportar macromoléculas a través de la barrera). Sin embargo, la intervención más universal, poética y científicamente validada sigue residiendo en nuestro propio movimiento.
Las directrices contemporáneas dictan que el esculpido cerebral requiere una prescripción polifacética:
-
Entrenamiento de resistencia (fuerza): Despierta el diálogo entre el músculo y el cerebro, demostrando ser el estímulo supremo para agudizar la atención y la toma de decisiones, especialmente entre los 65 y los 75 años.
-
Entrenamiento aeróbico: Eleva el flujo de sangre al hígado, maximizando la liberación de GPLD1, logrando que el cerebro parezca, biológicamente, casi un año más joven.
-
Prácticas mente-cuerpo: Afinan la flexibilidad del pensamiento lógico y la calma cognitiva.
Para quienes alcanzan la octava y novena década de vida, la combinación de estímulos aeróbicos y de fuerza constituye el verdadero elixir de la juventud mental.
Conclusión: El legado vivo en cada latido
La deslumbrante confirmación de este mecanismo por la Universidad de California refunda nuestra comprensión sobre el declive cognitivo. Nos enseña que para salvar la mente, primero debemos blindar la frontera vascular que la protege. Nos demuestra que un hígado enfermo o una musculatura marchita no son desgracias aisladas, sino preludios directos del apagamiento intelectual. Y nos brinda la esperanza tangible de que un día, a través de la farmacología, podremos devolver la dignidad mental a quienes sus cuerpos ya no pueden sostener.
Santiago Ramón y Cajal intuyó magistralmente que el cerebro no era una entidad pasiva condenada a la decadencia ineludible, sino una materia viva, plástica y sedienta de estímulo. Hoy, bajo la luz del microscopio electrónico y la biología molecular, sabemos que cada paso vigoroso, cada músculo tensado y cada latido acelerado, son las herramientas con las que el organismo envía a sus mensajeros protectores. El cerebro no es una isla; es el jardín más sublime del cuerpo, y la voluntad humana, a través del ejercicio, es su más devoto jardinero.
Invitamos a los espíritus curiosos a adentrarse en los pormenores de esta fascinante obra de la biología moderna, consultando la investigación original publicada en la revista científica Cell a través del siguiente enlace oficial: https://doi.org/10.1016/j.cell.2026.01.024
Liver exerkine reverses aging- and Alzheimer’s-related memory loss via vasculatureDescarga
Imagen de portada


Comentarios
Para activar los comentarios: ve a giscus.app, introduce el repositorio
joseadserias-dotcom/cajal-digitaly reemplaza los IDs ensrc/layouts/Articulo.astro.