El nombramiento de la neurocientífica Liset Menéndez de la Prida como nueva directora del Centro de Neurociencias Cajal (CNC) del CSIC no es solo un cambio de liderazgo; es la afirmación de una visión que conecta el legado fundacional de Santiago Ramón y Cajal con las fronteras más avanzadas de la ciencia del siglo XXI. Donde Cajal, armado con su microscopio y sus tinciones, nos legó los mapas estáticos de la “selva impenetrable” del cerebro, la Dra. Menéndez de la Prida, pertrechada con la física de los sistemas complejos, la neurotecnología y la inteligencia artificial, se adentra en esa misma selva para descifrar su dinámica: el lenguaje eléctrico, la sinfonía de ritmos que da origen a la memoria y la cognición. Su trabajo representa la evolución natural de la Doctrina de la Neurona, una traslación del plano anatómico al funcional, del estático al computacional. Este es un análisis profundo de la trayectoria científica que define a la nueva directora del Centro de Neurociencias Cajal (CNC), una investigación que persigue las leyes universales que gobiernan los circuitos neuronales en la salud y la enfermedad, perpetuando así la búsqueda de Cajal de los “arcanos de la vida” en la estructura íntima del sistema nervioso.
La Dra. Liset Menéndez de la Prida y su Laboratorio de Circuitos Neuronales

La investigación de la Dra. Liset Menéndez de la Prida y su Laboratorio de Circuitos Neuronales se erige en la confluencia de la física teórica, la neurobiología experimental y la ciencia de datos, impulsada por un objetivo central: comprender cómo la dinámica de los microcircuitos del hipocampo da a luz a la memoria. Su enfoque se cimienta sobre una convicción fundamental, expresada en sus propias palabras:
“Los mismos circuitos neuronales que asocian estímulo y respuesta, generan una expectativa temporal sobre la que construyes tus decisiones, y son los mismos circuitos que sacuden al epiléptico y que le impiden recordar lo que pasó”.
Este texto deconstruye la investigación seminal de su laboratorio sobre las oscilaciones neuronales, en particular las ondas agudas-rizos (Sharp-Wave Ripples, SWRs), el sustrato fisiológico para la consolidación de la memoria. A continuación, explora la trágica metamorfosis de estos ritmos fisiológicos en las cacofonías patológicas de la epilepsia del lóbulo temporal y la enfermedad de Alzheimer. Se pone un énfasis especial en el uso pionero de la neurotecnología y, de forma aún más significativa, en el desarrollo de nuevos paradigmas analíticos que, mediante el aprendizaje automático y la topología, buscan decodificar la geometría oculta en la actividad cerebral. Esta síntesis revela un programa de investigación que no solo desvela los mecanismos elementales de la memoria, sino que forja las herramientas y los marcos conceptuales que definirán el porvenir de la neurociencia de sistemas.
Sección 1: El Hipocampo: Arquitectura de un Recuerdo
Conoceremos el contexto biológico y conceptual para la obra del laboratorio. Detallar el papel insustituible del sistema hipocampo-entorrinal como el crisol de la memoria, sentando las bases de por qué esta estructura, dibujada con tanta maestría por Cajal, sigue siendo el epicentro de una investigación tan intensa.
1.1. Anatomía y Organización Funcional del Sistema Hipocampo-Entorrinal
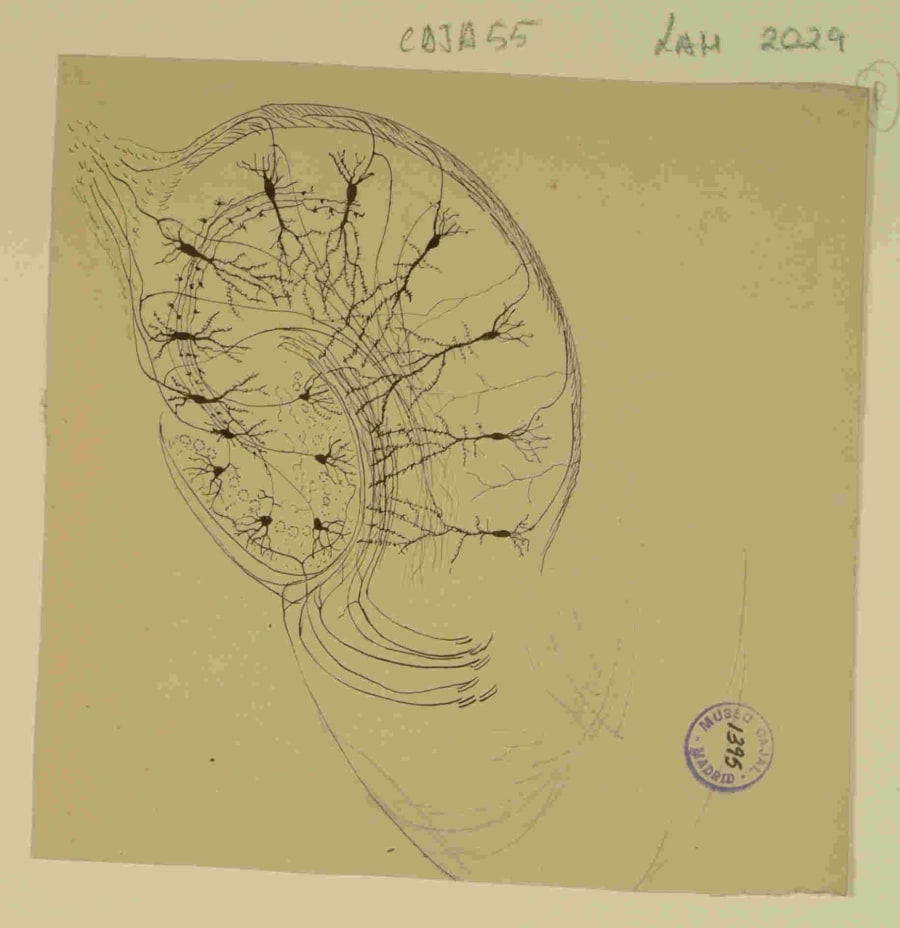
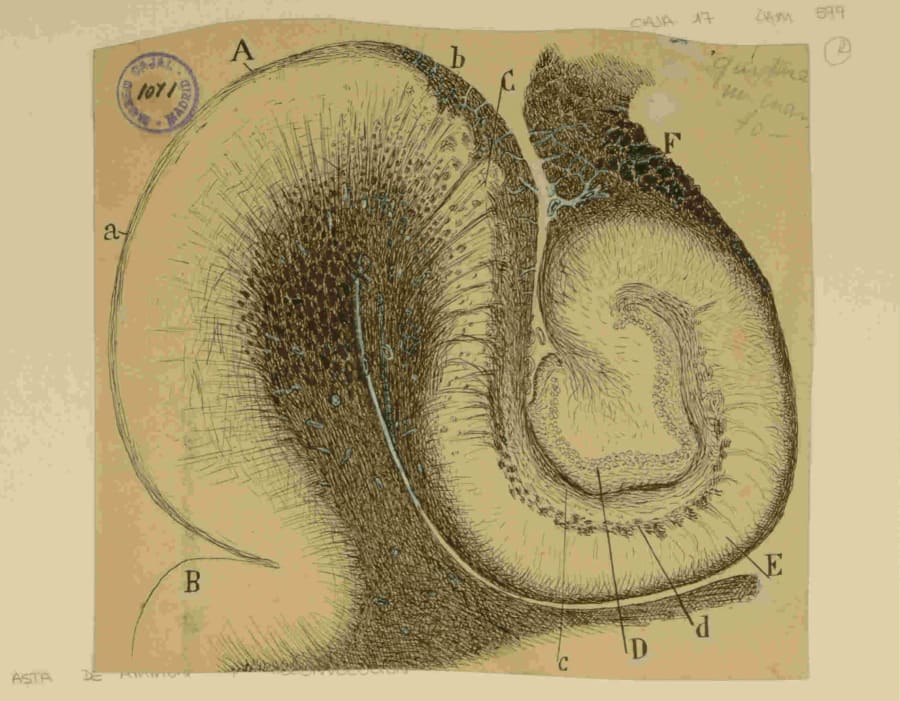
El hipocampo es una de las estructuras más conservadas en la filogenia de los mamíferos, un testimonio evolutivo de su función indispensable en la cognición. Es el núcleo de un sistema mayor que incluye la corteza entorrinal, con la que mantiene un diálogo bidireccional incesante, esencial para sus operaciones. Su organización interna, descrita canónicamente por el bucle trisináptico, es una obra maestra de la ingeniería biológica: una vía de procesamiento de información unidireccional que fluye desde la corteza entorrinal, atraviesa el giro dentado, la región CA3 y la región CA1, para finalmente retornar a la corteza. Esta arquitectura secuencial, un verdadero circuito lógico, es la clave de cómo el hipocampo procesa y segrega la información.
La arquitectura del hipocampo revela una notable división del trabajo: cada una de sus regiones o subcampos opera con una función específica y no redundante, actuando como componentes distintos de un circuito altamente especializado. La región CA3, con su densa red de conexiones recurrentes, actúa como una red autoasociativa, un “cuaderno de bocetos” neuronal capaz de completar patrones a partir de pistas fragmentarias, mecanismo esencial para la evocación de recuerdos. La región CA1, en cambio, funciona como el gran “curador” y principal centro de salida, comparando la información procesada en CA3 con la entrada directa de la corteza entorrinal. La investigación temprana de la Dra. Menéndez de la Prida ya se centró en la diversidad funcional de las neuronas del subículo, una estructura de salida clave, demostrando cómo distintos tipos celulares contribuyen de forma diferencial a los ritmos de la red.
Su localización en la profundidad del lóbulo temporal lo conecta íntimamente con el sistema límbico, permitiéndole teñir los recuerdos con contenido emocional, un componente vital de nuestra memoria autobiográfica. Sin embargo, esta posición privilegiada y su exquisita circuitería lo convierten también en un foco de vulnerabilidad, siendo el epicentro de patologías como la epilepsia del lóbulo temporal (ELT).
1.2. La Base Celular y de Red de la Memoria Episódica y Espacial
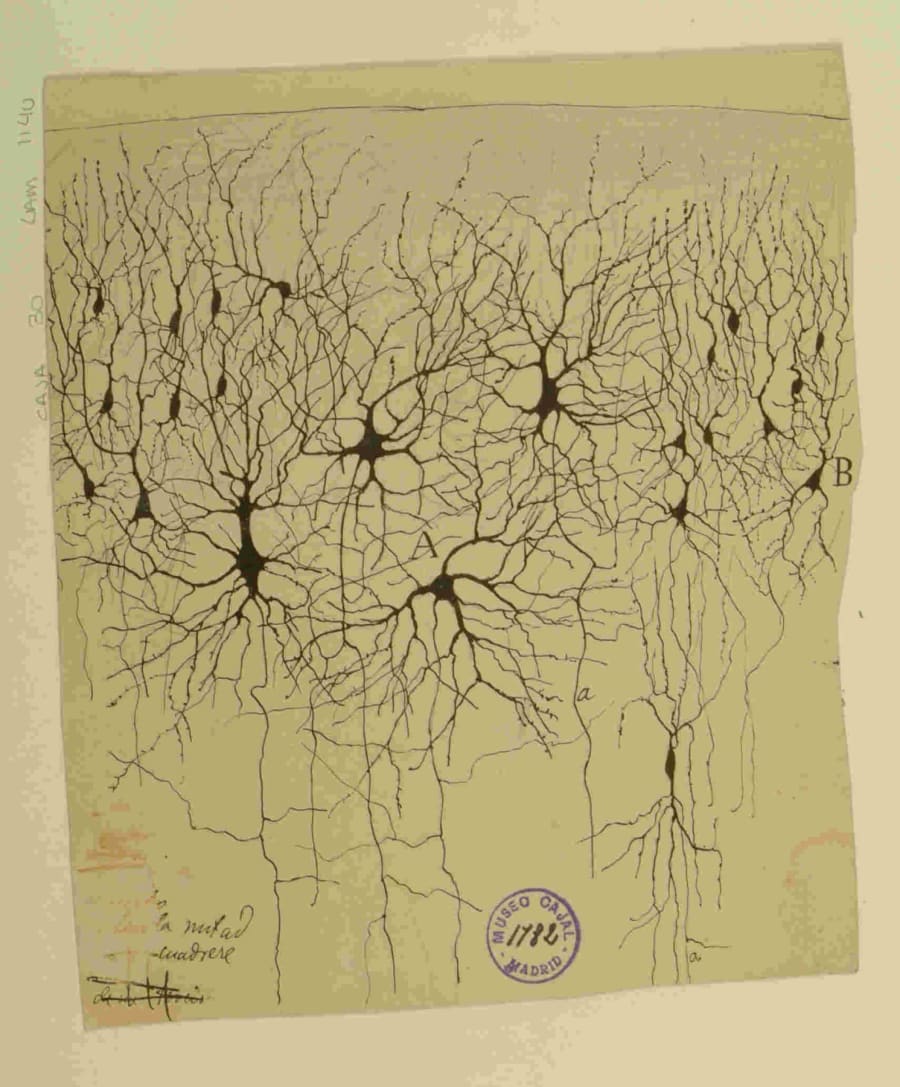
La función más celebrada del hipocampo es su papel en la formación de la memoria declarativa, que engloba tanto la memoria semántica (hechos) como la episódica. La memoria episódica es la capacidad de revivir eventos autobiográficos en su contexto espaciotemporal único —el “qué, dónde y cuándo” de nuestra existencia—, constituyendo el tejido de nuestra narrativa personal.
A nivel celular, esta función se sustenta en un código neuronal de asombrosa elegancia. El descubrimiento de las “células de lugar” en el hipocampo por John O’Keefe y las “células de red” en la corteza entorrinal por los Moser, galardonado con el Premio Nobel en 2014, revolucionó nuestra comprensión del espacio y la memoria. Las células de lugar se activan cuando un animal ocupa una posición específica, creando un mapa cognitivo interno del entorno. La propia Dra. Menéndez de la Prida ha subrayado la importancia capital de este hallazgo como pilar de la neurociencia moderna.
El proceso mnemónico es un continuo de tres actos: codificación, consolidación y recuperación. La codificación, o adquisición de nueva información, ocurre durante la vigilia activa, bajo el dominio de las oscilaciones theta. La consolidación, proceso central en la investigación del laboratorio, es la estabilización de la memoria para su almacenamiento a largo plazo, un diálogo nocturno entre el hipocampo y el neocórtex. Finalmente, la recuperación es el acto de acceder a la información, un proceso que vuelve a depender de los circuitos hipocampales.
1.3. El Hipocampo como Locus de Vulnerabilidad en la Enfermedad Neurológica
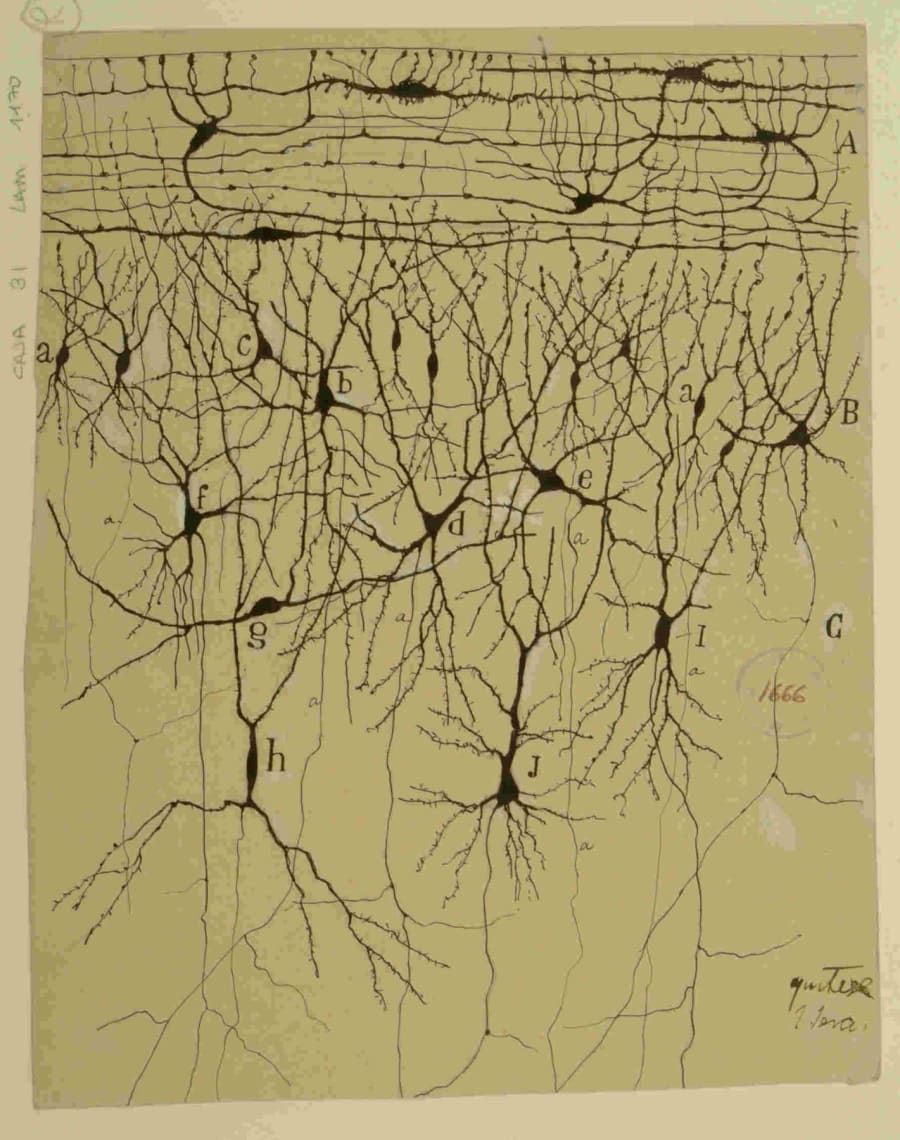
Las mismas propiedades que hacen del hipocampo una máquina de memoria casi perfecta lo convierten en un punto de extraordinaria fragilidad. La alta plasticidad sináptica y la densa conectividad recurrente crean un entorno de alta excitabilidad, un arma de doble filo: beneficiosa para la computación, pero que reduce el umbral para la actividad síncrona descontrolada que define a la epilepsia. La esclerosis hipocampal es el hallazgo patológico más común en pacientes con ELT farmacorresistente.
De forma análoga, el hipocampo es una de las primeras víctimas de la enfermedad de Alzheimer. La pérdida de memoria episódica, síntoma clínico inaugural de la enfermedad, es el eco de la disfunción temprana de sus circuitos. La patología de la EA, con sus placas de amiloide y ovillos de tau, ataca selectivamente las sinapsis del hipocampo, desmantelando su capacidad para forjar y guardar recuerdos.
Esta dualidad inherente del hipocampo —santuario de la memoria y foco de patología— es el principio organizador de la investigación de la Dra. Menéndez de la Prida. Su laboratorio no ve la salud y la enfermedad como estados discretos, sino como dos destinos posibles de las mismas propiedades fundamentales del circuito. La pregunta que unifica su obra es: ¿cuáles son las reglas que mantienen el equilibrio en la salud y cuál es el punto de inflexión que lo precipita hacia la patología?
Sección 2: Ritmos de la Cognición: El Papel Central de las Ondas Agudas-Rizos (SWRs)
Tránsito de la anatomía estática a la dinámica eléctrica que insufla vida a la función del hipocampo. Se presentan las oscilaciones cerebrales como el lenguaje de los circuitos neuronales, con un enfoque profundo en las SWRs como el fenómeno central de interés.
2.1. Decodificando las Oscilaciones Cerebrales: Un Lenguaje de los Circuitos Neuronales
La actividad cerebral no es un ruido aleatorio de disparos neuronales. Es una sinfonía coordinada de poblaciones de neuronas que generan actividad eléctrica rítmica y oscilatoria. Estos ritmos no son meros epifenómenos; son el mecanismo fundamental que organiza la actividad neuronal en el tiempo y el espacio, el andamiaje sobre el que se construyen la comunicación interregional y la computación cognitiva.
2.2. Una Inmersión Profunda en las Ondas Agudas-Rizos (SWRs): El Biomarcador Fisiológico de la Consolidación de la Memoria
Las ondas agudas-rizos (SWRs) son los eventos electrofisiológicos más sincrónicos del cerebro de los mamíferos, una verdadera explosión de actividad coordinada. Ocurren durante estados “offline”, como el reposo y el sueño de ondas lentas. El complejo SWR consta de una “onda aguda” de gran amplitud, originada por la descarga sincrónica de un vasto conjunto de neuronas en CA3, sobre la que cabalga una “ondulación” (ripple) de muy alta frecuencia (110-200 Hz) generada en CA1.
La función primordial de las SWRs es la consolidación de la memoria. Durante estos breves eventos, las secuencias de disparo neuronal que codificaron una experiencia se “reproducen” espontáneamente, pero a una velocidad comprimida, entre 10 y 20 veces más rápido que la experiencia original. Esta compresión temporal es un ingenioso mecanismo que permite a las reglas de la plasticidad sináptica operar con máxima eficacia, fortaleciendo las conexiones que sustentan el recuerdo y preparándolo para su almacenamiento a largo plazo. La interrupción experimental de las SWRs borra la memoria, confirmando su papel causal e indispensable.
2.3. El Modelo de Memoria de Dos Etapas y la Función Crítica “Offline” de las SWRs
El papel de las SWRs se formaliza en el influyente “modelo de memoria de dos etapas”. Este postula que la memoria a largo plazo se forja en dos actos:
-
Etapa 1 (Codificación): Durante la experiencia activa, el hipocampo actúa como un codificador rápido, formando representaciones frágiles de nuevos eventos.
-
Etapa 2 (Consolidación): Durante el reposo, las SWRs impulsan la reactivación de estas trazas de memoria. Este “ensayo nocturno” repetido y comprimido sirve para entrenar gradualmente al neocórtex, transfiriendo la información para su almacenamiento permanente. Las SWRs son, por tanto, el vehículo del diálogo hipocampo-neocortical que subyace a la consolidación.
La investigación del laboratorio de la Dra. Menéndez de la Prida va más allá, explorando la fina estructura de las SWRs. La reproducción no es una mera repetición; el cerebro recombina secuencias, permitiendo no solo la consolidación, sino la generalización, la abstracción y la planificación futura. Las SWRs no son un simple mecanismo de guardado, sino un sofisticado proceso computacional. Este enfoque eleva la electrofisiología al nivel de la “algorítmica neuronal”, buscando descifrar el código computacional inscrito en la dinámica eléctrica del cerebro.
Sección 3: La Mirada de un Físico sobre el Cerebro: El Núcleo Metodológico del Laboratorio
Enfatizaremos el enfoque interdisciplinario que define su trabajo y que constituye su contribución más singular al campo.
3.1. Una Trayectoria Interdisciplinaria: De los Sistemas Complejos a los Circuitos Neuronales
La trayectoria académica de la Dra. Menéndez de la Prida es la clave para entender la filosofía de su laboratorio. Licenciada en Física en La Habana, obtuvo su doctorado en Neurociencia en Alicante. Su interés original no era la biología, sino la física de los sistemas complejos. Como ella misma relata, su fascinación infantil por los huracanes del Caribe la llevó a las ecuaciones diferenciales que los modelan.
“Llegué a la neurociencia desde el interés por los sistemas complejos… Me interesaba la teoría del caos que se aplicaba al estudio de la oceanografía, la meteorología”.
La transición fue natural al reconocer en el cerebro el sistema complejo por excelencia.
Esta formación le inculcó una mentalidad que busca los primeros principios, la cuantificación rigurosa y las leyes universales que gobiernan la dinámica. En lugar de preguntar “¿qué neuronas se activan?”, su enfoque la lleva a preguntar “¿cuál es la estructura geométrica de la actividad poblacional?” o “¿cuáles son las ecuaciones de movimiento que gobiernan la transición entre estados de la red?“.
3.2. Integración de Técnicas Experimentales de Vanguardia
Para responder a estas preguntas, el laboratorio emplea una potente combinación de técnicas electrofisiológicas in vivo e in vitro. Este enfoque multi-escala es crucial para vincular las propiedades de neuronas individuales con la dinámica de red emergente que subyace a la cognición. Utilizan desde registros de alta densidad en animales que se comportan libremente hasta registros intracelulares tipo patch-clamp y, de manera crucial, trabajan con tejido cerebral humano procedente de cirugías de epilepsia, cerrando el círculo traslacional.
3.3. Pioneros en Neurotecnologías para la Interrogación de Circuitos de Alta Resolución
El laboratorio no solo utiliza herramientas, sino que las crea y las perfecciona. Su trabajo con optrodos de μLED de alta densidad, que combinan la estimulación optogenética con el registro eléctrico de alta resolución, les permite una manipulación causal de los circuitos con una precisión espaciotemporal sin precedentes. Su participación en el desarrollo de sondas plasmónicas para la detección de neurotransmisores demuestra un compromiso con la superación de las barreras tecnológicas. Este impulso por la innovación es una consecuencia directa de su enfoque de físico: para medir un sistema complejo, se necesitan herramientas de medición cada vez más sofisticadas.
Sección 4: Cuando los Ritmos Fallan: Dinámicas del Hipocampo en la Enfermedad
Análisis del aspecto traslacional de la investigación, centrándonos en cómo la delicada sinfonía de las oscilaciones del hipocampo se convierte en la cacofonía de la enfermedad.
4.1. El Hipocampo Epiléptico: De Rizos Fisiológicos a Biomarcadores Patológicos
Un eje central del laboratorio es desentrañar los mecanismos de la ELT. Han sido pioneros en demostrar cómo las SWRs fisiológicas, cruciales para la memoria, se transforman en oscilaciones patológicas de alta frecuencia (pHFOs), o “rizos rápidos”, un biomarcador del tejido epileptogénico. Esta transición implica un colapso del delicado equilibrio entre excitación e inhibición. Específicamente, han identificado que un fallo en la inhibición perisomática, mediada por interneuronas de cesta, es un factor crucial. En la epilepsia, este freno inhibitorio se debilita, permitiendo que la excitación se propague sin control, dando lugar a la descarga hipersincrónica y desorganizada de los rizos rápidos.
4.2. Mecanismos del Deterioro de la Memoria en la Epilepsia
El laboratorio ha proporcionado una explicación mecanicista directa de la amnesia en la ELT. En el cerebro epiléptico, la reproducción ordenada de secuencias durante las SWRs se descompone. En lugar de una reactivación selectiva, un número mucho mayor de neuronas dispara de forma indiscriminada y “promiscua”. Este “desorden” del código neuronal corrompe la información que se está consolidando. De manera crucial, han demostrado que la restauración farmacológica de la precisión de este disparo neuronal mejora el rendimiento de la memoria en ratas epilépticas, abriendo una nueva y prometedora vía terapéutica.
4.3. Alteraciones de las SWRs como Sistema de Alerta Temprana en la Enfermedad de Alzheimer
El laboratorio extiende su conocimiento de las SWRs a la enfermedad de Alzheimer, donde han demostrado que estas oscilaciones se ven afectadas en etapas muy tempranas, a menudo antes de que los déficits de memoria sean evidentes. Las alteraciones incluyen una reducción en su tasa, una disminución de su potencia y, críticamente, una descoordinación temporal con las oscilaciones corticales, rompiendo el diálogo hipocampo-neocortical esencial para la consolidación. Esto posiciona a la disrupción de las SWRs como un potente biomarcador electrofisiológico temprano de la disfunción de la red en la EA.
El trabajo del laboratorio propone un “espectro de sincronicidad”: en un extremo, la sincronicidad óptima y rica en información de las SWRs fisiológicas; en el otro, la hipersincronía patológica de la epilepsia. La actividad en la EA se situaría en un punto intermedio de sincronicidad degradada. Esta visión redefine el diagnóstico neurológico, permitiendo no solo detectar, sino cuantificar la gravedad de la enfermedad a nivel de circuito.
Sección 5: La Nueva Frontera: Desvelando la Geometría de la Memoria con Ciencia de Datos e IA
El aspecto más vanguardista de la investigación del laboratorio: la aplicación de la ciencia de datos y la IA para revolucionar el análisis de los datos neuronales, un verdadero cambio de paradigma.
5.1. Más Allá del Análisis Espectral: La Necesidad de un Nuevo Paradigma Analítico
El análisis tradicional de las señales cerebrales, basado en frecuencias, es insuficiente para capturar la rica estructura de eventos complejos como las SWRs. La llegada de registros de alta densidad ha creado un desafío de “big data” que exige herramientas analíticas más potentes y automatizadas.
5.2. El Proyecto DeepCode: Aplicando el Análisis Topológico de Datos para Revelar la “Forma” de la Memoria
La contribución más novedosa del laboratorio es el uso del Análisis Topológico de Datos (TDA), una rama de las matemáticas que estudia la “forma” de los datos. En lugar de analizar la forma de onda, el enfoque TDA representa cada SWR como un punto en un espacio matemático de alta dimensión. Al agregar miles de SWRs, se forma una “nube de puntos”. Su descubrimiento clave, publicado en Nature Neuroscience, fue que esta nube tiene una estructura geométrica específica y continua. La posición de cada SWR en esta nube no es aleatoria; codifica características de la forma de onda. Este método proporciona una forma completamente nueva de clasificar las SWRs, un “microscopio” matemático para observar la forma de los eventos de memoria y diferenciar robustamente las formas fisiológicas de las patológicas.
5.3. Una Caja de Herramientas Inter-especie: Usando el Aprendizaje Automático para Estandilizar el Análisis
El laboratorio ha desarrollado una caja de herramientas de modelos de aprendizaje automático, basados en Redes Neuronales Convolucionales (CNNs), para la detección automatizada de SWRs. Un logro fundamental es su generalización inter-especie: modelos entrenados con datos de ratón detectan con éxito SWRs en macacos, revelando principios conservados en la evolución de los mamíferos. Esta caja de herramientas, de código abierto, promueve la estandarización y la reproducibilidad en el campo.
5.4. De los Datos a la Comprensión: Cómo los Modelos de IA Proporcionan Nuevas Interpretaciones
El laboratorio va más allá de usar la IA como una “caja negra”. Mediante técnicas de “IA interpretable”, interrogan a las redes para comprender qué características de la señal están utilizando. En palabras de la Dra. Menéndez de la Prida, este enfoque permite que “el dato es el que habla”. Este método “impulsado por los datos” permite que los propios datos revelen las características más importantes, en lugar de depender de definiciones humanas, que pueden ser sesgadas. Este trabajo ejemplifica un poderoso bucle de retroalimentación. “Es como cerrar un círculo”, explica, “la IA se inspira en el cerebro y, a su vez, nos ayuda a entender el cerebro”. Su laboratorio no solo usa la IA, sino que descubre principios computacionales de la inteligencia biológica que podrían informar el futuro de la inteligencia artificial.
Sección 6: Horizontes Futuros: El Legado en Marcha
Síntesis de los temas anteriores y proyección de la visión de la Dra. Menéndez de la Prida para el futuro de la neurociencia y del Centro de Neurociencias Cajal (CNC).
6.1. Potencial Traslacional: Las SWRs como Dianas Diagnósticas y Terapéuticas
La culminación de esta investigación apunta a un futuro con un inmenso potencial clínico. La capacidad de clasificar las SWRs con IA abre la puerta a su uso como biomarcadores ultrasensibles para el diagnóstico precoz y el seguimiento de la epilepsia y la EA. Más allá del diagnóstico, el trabajo apunta a nuevas terapias. La restauración de la integridad de las SWRs en modelos animales sugiere que podrían ser un objetivo terapéutico directo. Se pueden vislumbrar futuros sistemas de neuroestimulación de bucle cerrado que “editen” los ritmos cerebrales en tiempo real para restaurar la función fisiológica, un enfoque de una sofisticación muy superior a los tratamientos actuales.
6.2. La Visión de un Futuro Impulsado por los Datos, Colaborativo e Interdisciplinario
La Dra. Menéndez de la Prida aboga por una ciencia cada vez más “impulsada por los datos”, donde los grandes conjuntos de datos guíen el descubrimiento. Enfatiza que la complejidad del cerebro exige una integración profunda de múltiples disciplinas. “En el mundo de hoy, el que crea que solo un ingeniero o solo un biólogo o solo un matemático va a ser capaz de resolver los problemas… se equivoca”.
Su impacto se extiende más allá de su laboratorio. Asume un papel activo en la construcción del ecosistema científico del futuro. Sus roles de liderazgo, como la Presidencia del Comité de Programa de la Federación de Sociedades Europeas de Neurociencia (FENS), y sus funciones editoriales en revistas de primer nivel, le permiten dar forma a la dirección del campo y fomentar lo que ella llama “un sentido de comunidad”. Al desarrollar y compartir herramientas de código abierto, invierte en las “obras públicas” de la ciencia, construyendo la infraestructura que permitirá el progreso de toda la comunidad. Esta contribución estratégica la posiciona no solo como una investigadora principal, sino como una arquitecta de ecosistemas que está dando forma activa a la próxima generación de la neurociencia, asegurando que el legado de Cajal no solo se preserve, sino que florezca en la nueva era del descubrimiento.
Apéndice
Tabla 1: Publicaciones Emblemáticas del Laboratorio de la Prida
Publicación (Título, Revista, Año)Pregunta de InvestigaciónMetodología Clave****Hallazgo/ Contribución PrincipalTopological analysis of sharp-wave ripple waveforms reveals input mechanisms behind feature variations. Nat Neurosci, 2023.¿Puede la estructura matemática de las formas de onda de las SWRs revelar los mecanismos de circuito subyacentes que las generan?Análisis Topológico de Datos (TDA)Las SWRs forman una estructura geométrica continua (“nube de puntos”) en un espacio de alta dimensión. La posición dentro de esta nube codifica características de la forma de onda que se correlacionan con diferentes entradas sinápticas, proporcionando una nueva forma de clasificar los eventos.A machine learning toolbox for the analysis of sharp-wave ripples reveals common waveform features across species. Commun Biol, 2024.¿Se pueden desarrollar modelos de aprendizaje automático para detectar y analizar SWRs de forma robusta y generalizable entre especies?Redes Neuronales Convolucionales (CNNs), CrowdsourcingSe desarrolló una caja de herramientas de código abierto con modelos de ML que detectan una amplia diversidad de SWRs. Los modelos generalizan de ratones a macacos, revelando características de SWRs conservadas evolutivamente.Deep learning based feature extraction for prediction and interpretation of sharp-wave ripples in the rodent hippocampus. eLife, 2022.¿Cómo pueden las redes de aprendizaje profundo identificar SWRs y qué características fisiológicas aprenden a reconocer?CNNs, IA InterpretableLas CNNs identifican SWRs automáticamente a partir de registros LFP. El análisis de la red revela que aprende a especializarse en características fisiológicas clave como oscilaciones, deflexiones y descargas poblacionales sincrónicas.Inhibitory conductance controls place field dynamics in the hippocampus. Cell Reports, 2022.¿Cuál es el papel de la inhibición en la configuración de la dinámica de los campos de lugar de las neuronas del hipocampo?Registros in vivo intracelulares y extracelularesLa conductancia inhibitoria controla dinámicamente el tamaño y la forma de los campos de lugar, lo que sugiere un mecanismo para la flexibilidad del código espacial.Determinants of different deep and superficial CA1 pyramidal cell dynamics during sharp-wave ripples. Nat Neurosci, 2015.¿Por qué diferentes subpoblaciones de neuronas piramidales en CA1 (profundas vs. superficiales) participan de manera diferente en las SWRs?Registros in vivo y modelado computacionalLas células piramidales profundas y superficiales reciben diferentes equilibrios de excitación e inhibición durante las SWRs, lo que explica su participación diferencial y sugiere canales de información paralelos para la consolidación de la memoria.Emergent dynamics of fast ripples in the epileptic hippocampus. J Neurosci, 2010.¿Cómo surgen las oscilaciones patológicas de alta frecuencia (rizos rápidos) en el hipocampo epiléptico?Registros in vivo y modelos computacionalesLos rizos rápidos emergen de la dinámica de la red epiléptica y se correlacionan con una degradación de la precisión temporal del disparo neuronal, lo que los vincula con los déficits de memoria.
Tabla 2: Análisis Comparativo de las Oscilaciones de Alta Frecuencia del Hipocampo
Característica****SWRs Fisiológicas (Cerebro Sano)****Rizos Rápidos Patológicos (Epilepsia)****SWRs Alteradas (Modelos de Alzheimer)****Banda de Frecuencia~110-200 Hz (en roedores)>250 HzFrecuencia a menudo reducida o espectro alteradoDuración~50-100 msTípicamente más cortosDuración puede estar reducidaCorrelatos CelularesDisparo escaso y selectivo de células piramidales; fuerte control inhibitorio.Disparo hipersincrónico y promiscuo de células piramidales; colapso de la inhibición.Aumento de la participación neuronal, alteración del equilibrio excitación/inhibición.Relación con la MemoriaEsencial para la consolidación de la memoria a través de la reproducción neuronal ordenada.Interfiere con la consolidación de la memoria al “desordenar” la reproducción neuronal.Asociado con déficits de memoria; la consolidación está deteriorada.Relación con la PatologíaFenómeno fisiológico normal.Biomarcador del tejido epileptogénico; contribuye a la epileptogénesis.Biomarcador temprano de la disfunción de la red; precede a los déficits de comportamiento.
Bibliografía
-
Sebastian, E. R., Quintanilla, J. P., Sánchez-Aguilera, A., Esparza, J., Cid, E., & de la Prida, L. M. (2023). Topological analysis of sharp-wave ripple waveforms reveals input mechanisms behind feature variations. Nature Neuroscience, 26, 2171–2181. DOI: 10.1038/s41593-023-01471-9
-
Navas-Olive, A., Rubio, A., Abbaspoor, S., Hoffman, K. L., & de la Prida, L. M. (2024). A machine learning toolbox for the analysis of sharp-wave ripples reveals common waveform features across species. Communications Biology, 7, 211. DOI: 10.1038/s42003-024-05871-w
-
Navas-Olive, A., Amaducci, R., Jurado-Parras, M. T., Sebastian, E. R., & de la Prida, L. M. (2022). Deep learning-based feature extraction for prediction and interpretation of sharp-wave ripples in the rodent hippocampus. eLife, 11, e77772. DOI: 10.7554/eLife.77772
-
Valero, M., Navas-Olive, A., de la Prida, L. M., & Buzsaki, G. (2022). Inhibitory conductance controls place field dynamics in the hippocampus. Cell Reports, 40(8), 111232. DOI: 10.1016/j.celrep.2022.111232
-
Valero, M., Cid, E., Averkin, R. G., Aguilar, J., Sanchez-Aguilera, A., Viney, T. J., Gomez-Dominguez, D., & Menendez de la Prida, L. (2015). Determinants of different deep and superficial CA1 pyramidal cell dynamics during sharp-wave ripples. Nature Neuroscience, 18(9), 1211-1213. DOI: 10.1038/nn.4074
-
Inostroza, M., Brotons-Mas, J. R., Laurent, F., Cid, E., & de la Prida, L. M. (2013). Specific impairment of “what-where-when” episodic-like memory in experimental models of temporal lobe epilepsy. Journal of Neuroscience, 33(45), 17749-17762. DOI: 10.1523/JNEUROSCI.0957-13.2013
-
Ibarz, J. M., Foffani, G., Cid, E., Inostroza, M., & Menendez de la Prida, L. (2010). Emergent dynamics of fast ripples in the epileptic hippocampus. Journal of Neuroscience, 30(48), 16249-16261. DOI: 10.1523/JNEUROSCI.3357-10.2010
Portada



Comentarios
Para activar los comentarios: ve a giscus.app, introduce el repositorio
joseadserias-dotcom/cajal-digitaly reemplaza los IDs ensrc/layouts/Articulo.astro.